Приключения Мистера Томпкинса, стр. 32
Наконец, физики осознали, в чем именно заключается слабая сторона теории Бора: вместо основательной перестройки классической механики теория Бора просто наложила ограничения на ее результаты, введя дополнительные условия, в принципе чуждые всей структуре классической теории. Правильное решение всей проблемы было получено лишь тринадцать лет спустя в виде так называемой волновой механики, изменившей самые основы классической механики в соответствии с новым квантовым принципом. Несмотря на то, что на первый взгляд система волновой механики может показаться еще более «сумасшедшей», чем теория Бора, эта новая микромеханика представляет собой одну из наиболее последовательных и признанных частей современной теоретической физики. Поскольку фундаментальный принцип новой механики и, в частности, понятия «неопределенность» и «расплывание траекторий» были рассмотрены мной в одной из предыдущих лекций, я обращаюсь теперь к вашей памяти или к вашим конспектам и хотел бы вернуться к проблеме строения атома. На схеме, которую вы сейчас увидите (следующий слайд, пожалуйста!) (см. рис. внизу), изображено движение атомных электронов, рассматриваемое с позиций волновой механики, или с точки зрения «расплывания орбит». Вы видите здесь те же самые типы движения, которые в рамках классической теории были представлены на предыдущем слайде (единственное различие состоит лишь в том, что по чисто техническим причинам каждый тип движения теперь изображен отдельно), но вместо четких линий, изображающих траектории в теории Бора, теперь перед нами расплывчатые пятна в полном согласии с фундаментальным принципом неопределенности. Различные состояния движения имеют такие же обозначения, как на предыдущем слайде, и сравнивая оба слайда, вы заметите, если слегка напряжете воображение, что расплывчатые облака на втором слайде очень точно передают общие характерные особенности старых орбит Бора.
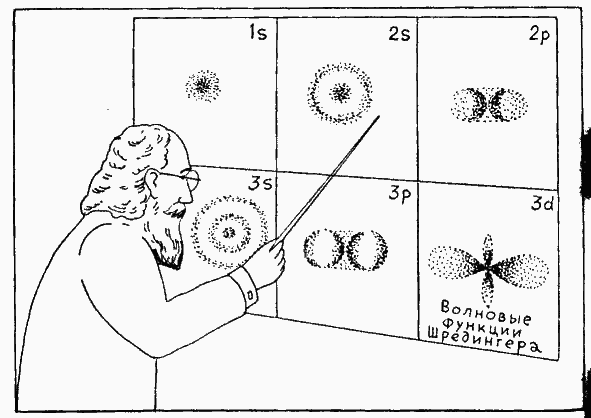
Оба слайда отчетливо показывают, что происходит с добрыми старомодными траекториями классической механики, когда в игру вступает квант, и хотя человеку непосвященному все это может показаться фантастическим сном, ученые, работающие в микрокосмосе атомов, не испытывают особых трудностей в восприятии такой картины.
Завершив на этом краткий обзор возможных состояний движения в электронной атмосфере атома, мы обращаемся теперь к важной проблеме, касающейся распределения различных атомных электронов по различным допустимым состояниям движения. Здесь мы сталкиваемся с новым принципом, совершенно незнакомым в макроскопическом мире. Этот принцип впервые был сформулирован моим молодым другом Вольфгангом Паули. Он утверждает, что в сообществе электронов данного атома никакие два электрона не обладают движением одного и того же типа. Это ограничение не имело бы особого значения, если бы число возможных движений было бесконечно велико, как в классической механике. Но поскольку правила квантования существенно уменьшают число «разрешенных» состояний движения, принцип Паули играет очень важную роль в атомном мире: он обеспечивает более или менее равномерное распределение электронов вокруг атомного ядра и мешает электронам скапливаться в каком-то одном месте.
Но из приведенной выше формулировки нового принципа не следует делать вывода о том, что расплывчатые квантовые состояния движения, изображенные на втором слайде, могут быть «заняты» только одним электроном. Действительно, помимо движения по орбите каждый электрон обладает спином, т.е. вращается вокруг собственной оси, и доктора Паули отнюдь не разочарует, если два электрона окажутся на одной орбите, если их спины будут направлены в противоположные стороны. Исследование спина электронов показывает, что скорость вращения электронов вокруг собственной оси всегда одна и та же и что направление спина всегда должно быть перпендикулярно плоскости орбит. Это означает, что возможны только два различных направления спина, которые соответственно можно считать происходящими «по часовой стрелке» и «против часовой стрелки».
Таким образом, применительно к квантовым состояниям принцип Паули может быть сформулирован следующим образом: в каждом квантовом состоянии движения могут находиться не более двух электронов, спины которых должны быть направлены в противоположные стороны. Проходя всю естественную последовательность элементов к атомам со все большим и большим числом электронов, мы обнаружим, что различные квантовые состояния движения постепенно заполняются электронами и диаметр атома монотонно возрастает. В этой связи нельзя не упомянуть о том, что с точки зрения силы связи различные квантовые состояния атомных электронов могут быть объединены в отдельные группы (или оболочки) с приблизительно равной силой связи. По мере продвижения вдоль естественной последовательности элементов, мы видим, что одна группа заполняется за другой и в результате последовательного заполнения электронных оболочек свойства атомов периодически изменяются. Это объясняет хорошо известную периодичность свойств элементов, открытую эмпирически знаменитым русским химиком Дмитрием Ивановичем Менделеевым.
Глава 12
Внутри ядра
Следующая лекция, которую посетил мистер Томпкинс, была посвящена внутреннему строению ядра как центра, вокруг которого вращаются атомные электроны.
— Леди и джентльмены, — начал профессор. — Все более углубляясь в строение материи, мы попытаемся теперь проникнуть нашим мысленным взором внутрь ядра, в загадочную область, занимающую лишь одну тысячную от миллиардной доли общего объема атома. И все же, несмотря на столь невероятно малые размеры новой области наших иссследований, мы обнаружили в ней самую оживленную деятельность. Ведь атомное ядро — сердце атома, и именно в нем, несмотря на сравнительно малые размеры, сосредоточено 99,97% всей массы атома.
Вступая в область атомного ядра после сравнительно бедно населенной электронной атмосферы атома, мы сразу же будем поражены ее необычной перенаселенностью. Если электроны атомной атмосферы движутся в среднем на расстояниях, превышающих их собственный диаметр примерно в несколько тысяч раз, то частицы, живущие внутри ядра, буквально теснились бы плечом к плечу, будь у них плечи. В этом смысле картина, которая открывается нам внутри ядра, очень напоминает картину обыкновенной жидкости с тем лишь различием, что внутри ядра мы вместо молекул встречаем гораздо более мелкие и гораздо более элементарные частицы, известные под названием протоны и нейтроны. Уместно заметить, что, несмотря на различные имена, протоны и нейтроны можно рассматривать просто как два различных зарядовых состояния одной и той же тяжелой элементарной частицы, известной под названием нуклон. Протон представляет собой положительно заряженный нуклон, нейтрон — электрически нейтральный нуклон. Не исключена возможность, что существуют также отрицательно заряженные нуклоны, хотя их пока никто не наблюдал. Что касается их геометрических размеров, нуклоны не слишком отличаются от электронов: диаметр нуклона составляет около 0,000 000 000 0001 см. Однако нуклоны гораздо тяжелее: на чашках весов протон или нейтрон можно уравновесить 1840 электронами. Как я уже говорил, частицы, образующие атомное ядро, упакованы очень плотно и это объясняется действием особых ядерных сил сцепления, аналогичных силам, действующим между молекулами в жидкости. Так же как в жидкости силы ядерного сцепления не дают нуклонам полностью отделиться друг от друга, но не мешают относительным перемещениям нуклонов. Таким образом, ядерная материя в какой-то степени обладает текучестью и, не будучи возмущаема внешними силами, принимает форму сферической капли, как обычная капля жидкости. На схеме, которую я вам сейчас покажу, условно изображены различные типы атомных ядер, образованных из протонов и нейтронов. Простейшее ядро водорода состоит всего лишь из одного протона, в то время как самое сложное ядро урана состоит из 92 протонов и 142 нейтронов. Разумеется, разглядывая эти картинки, не следует упускать из виду, что перед вами лишь весьма условные изображения реальных ядер, поскольку в силу фундаментального принципа неопределенности квантовой теории положение каждого нуклона в действительности «размазано» по всему объему ядра.
