Физика для всех. Молекулы, стр. 36
Химическую реакцию, идущую с выделением тепла, можно моделировать картинкой, приведенной на рис. 7.1. Шарик вкатывается на горку, переваливает через барьер и скатывается вниз. Поскольку начальный уровень выше конечного, то энергии потратится меньше, чем выделится.
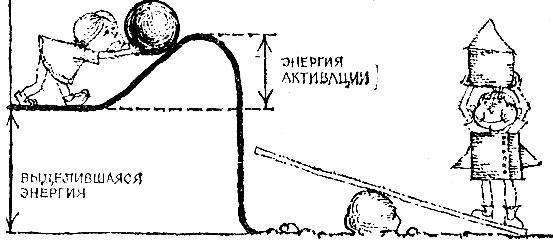
Рис. 7.1
Эта модель наглядно иллюстрирует причину резкой зависимости скорости реакции от температуры. Если температура мала, то "скорость шара" недостаточна, чтобы забраться на гору. По мере роста температуры все более и более будет расти число шариков, которые будут перемахивать через горку. Скорости химических реакций очень сильно зависят от температуры. Как правило, повышение температуры на 10 градусов увеличивает скорость реакции в 2-4 раза. Если скорость реакции увеличивается, скажем, в 3 раза при повышении температуры на 10 градусов, то повышение температуры на 100 градусов дает увеличение в 310?60 000 раз, на 200 градусов - уже в 320?4*109, а на 500 градусов- в З50, т. е. примерно в 1024 раз. Неудивительно, что реакция, которая идет с нормальной скоростью при температуре 500°С, при комнатной температуре не происходит вообще.
Горение и взрыв
Для того чтобы началось горение, надо, как известно, поднести к горючему предмету горящую спичку. Но и спичка не зажигается сама, ею надо чиркнуть о коробку. Таким образом, для того чтобы началась такая химическая реакция, необходимо предварительное нагревание. Поджигание создает в начальный момент необходимую для реакции температуру. Дальше высокую температуру поддерживает уже тепло, которое выделяется при реакции.
Начальный местный подогрев должен быть достаточен для того, чтобы выделение тепла при реакции превышало теплоотдачу в окружающую холодную среду. Поэтому каждая реакция имеет свою, как говорят, температуру воспламенения. Горение начинается, только если начальная температура выше температуры воспламенения. Например, температура воспламенения дерева 610°С; бензина - около 200°С, белого фосфора - 50°С.
Горение дров, угля или нефти - это химическая реакция соединения этих веществ с кислородом воздуха. Поэтому такая реакция идет с поверхности: пока не выгорит внешний слой, следующий не может принять участие в горении. Этим и объясняется относительная медленность горения. В справедливости сказанного нетрудно убедиться на практике. Если размельчать горючее, то скорость горения можно значительно увеличить. Для этой цели во многих печных устройствах производится распыление угля в топках.
Так же размельчается и смешивается с воздухом топливо в цилиндре мотора. Горючим в моторе служит не уголь, а более сложные вещества, например, бензин. Молекула октана, входящего в состав этого вещества (рис. 7.2 слева), состоит из 8 атомов углерода и 18 атомов водорода, соединенных так, как показано на рисунке. При горении эта молекула подвергается ударам кислородных молекул. Встречи с молекулами кислорода разрушают молекулу октана. Силы, соединяющие в молекуле октана один или два атома углерода с атомом водорода, а также силы, соединяющие два атома кислорода в молекулу кислорода, не могут -противостоять более, сильному, как говорят химики, "сродству" между атомами кислорода, с одной стороны, и атомами' углерода и водорода - с другой. Поэтому старые связи между атомами молекул нарушаются, атомы перегруппировываются и создают новые молекулы. Как показывает рис. 7.2 справа, новыми молекулами - продуктами горения - и в этом случае являются углекислый газ и вода. Вода при этом образуется в форме пара,
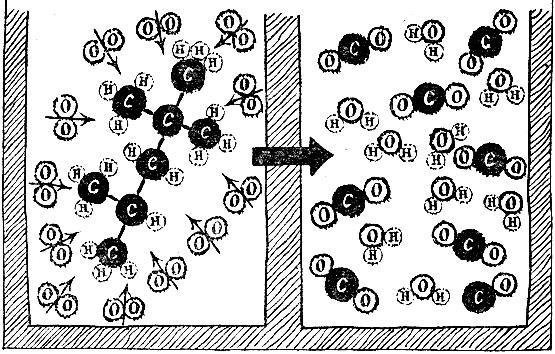
Рис. 7.2
Совершенно иначе обстоит дело в том случае, когда воздушная атмосфера не нужна, а все необходимое для реакции содержится внутри вещества. Примером такого вещества является смесь водорода с кислородом (ее называют гремучим газом). Реакция идет не с поверхности, а происходит1 внутри вещества. В отличие от случая горения вся энергия, образующаяся при реакции, отдается почти мгновенно, вследствие этого резко повышается давление и происходит взрыв. Гремучий газ не горит, а взрывается.
Итак, взрывчатое вещество должно содержать внутри себя атомы или молекулы, нужные для реакции. Понятно, что можно приготовить взрывающиеся газовые смеси. Существуют и твердые взрывчатые вещества. Они являются взрывчатыми именно потому, что в их состав входят все атомы, необходимые для химической реакции, дающей тепло и свет.
Химическая реакция, происходящая при взрыве,- это реакция распада, расщепления молекулы на части. На рис. 7.3 показана для примера взрывная реакция - расщепление на части молекулы нитроглицерина. Как видно на правой части схемы, из исходной молекулы образуются молекулы углекислого газа, воды, азота. В составе продуктов реакции мы находим обычные продукты горения, но горение произошло без участия молекул кислорода воздуха - все необходимые для горения атомы содержатся внутри молекулы нитроглицерина.
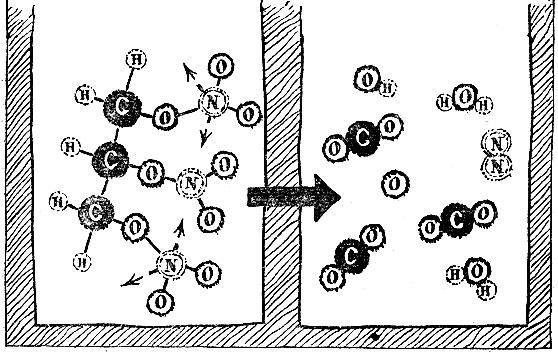
Рис. 7.3
Как распространяется взрыв по взрывчатому веществу, например гремучему газу? Когда поджигают взрывчатое вещество, возникает местный нагрев. Реакция происходит в нагретом объеме. Но при реакции выделяется тепло, которое путем теплопередачи переходит в соседние слои смеси. Этого тепла достаточно для того, чтобы и в соседнем слое произошла реакция. Вновь выделившееся тепло поступит в следующие слои гремучего газа, и так со скоростью, связанной с передачей тепла, реакция распространяется по всему веществу. Скорость такой передачи - порядка 20-30 м/с. Разумеется, это очень быстро. Метровая трубка с газом взрывается за 1/20 с, т. е. почти мгновенно, в то время как скорость горения дров или кусков углей, происходящего с поверхности, а не в объеме, измеряется сантиметрами в минуту, т. е. в несколько тысяч раз меньше.
Тем не менее можно назвать и этот взрыв медленным, так как возможен другой взрыв, в сотни раз более быстрый, чем описанный.
Быстрый взрыв вызывается ударной волной. Если в каком-либо слое вещества резко повышается давление, то от этого места начнет распространяться фронт повышенного давления. В этом случае и говорят об ударной волне. Эта волна приводит к значительному скачку температуры, который передается от слоя к слою. Повышение температуры дает начало взрывной реакции, а взрыв приводит к повышению давления и поддерживает ударную волну, интенсивность которой иначе быстро падала бы по мере ее распространения. Таким образом, ударная волна вызывает взрыв, а взрыв в свою очередь поддерживает ударную волну.
Описанный нами взрыв называется детонацией. Так как детонация распространяется по веществу со скоростями ударной волны (порядка 1 км/с), то она действительно быстрее "медленного" взрыва в сотни раз.
Какие же вещества взрываются "медленно", а какие "быстро"? Так ставить вопрос нельзя: одно и то же вещество, находящееся в разных условиях, может и взрываться "медленно" и детонировать, а в некоторых случаях "медленный" взрыв переходит в детонацию.
Некоторые вещества, например йодистый азот, взрываются от прикосновения соломинки, от небольшого нагревания, от световой вспышки. Такое взрывчатое вещество, как тротил, не взрывается, если его уронить, даже если его прострелить из винтовки. Для взрыва требуется сильная ударная волна.
Существуют вещества, еще менее чувствительные к внешним воздействиям. Удобрительная смесь аммиачной Селитры и сернокислого аммония не считалась взрывчатой до трагического случая, происшедшего в 1921 г. на немецком химическом заводе в Оппау. Для дробления слежавшейся смеси там был применен взрывной способ. В результате на воздух взлетели склад и весь завод. В несчастье нельзя было упрекать инженеров завода: примерно двадцать тысяч подрывов прошло нормально и лишь один раз создались условия, благоприятные для детонации.
