Белые пятна безбрежного океана, стр. 16
Как строится молекула воды
Вспомним, что вероятностное нахождение электрона по отношению к ядру определяется электронным облаком, т. е. совокупностью всех точек пространства, через которые может пробежать электрон. Это воображаемое облако называют орбиталью. Установлено: на одной орбитали не может находиться одновременно более двух электронов.
Единственный электрон атома водорода (1 s1) имеет орбиталь в виде сферы. Такая форма орбитали соответствует минимально возможному уровню энергии атома.
В атоме кислорода все гораздо сложнее. Атом кислорода имеет два слоя электронов. Внутренний (слой К.) укомплектован двумя s-электронами, вращающимися по сферической орбитали (условное обозначение этих электронов 1 s2, где 1 - номер слоя, s - энергетическое состояние - орбиталь, 2 - количество электронов на орбитали).
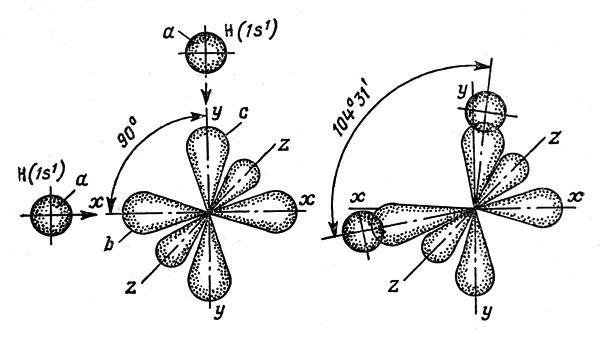
Рис. 10. Схема образования молекулы Н2О. Сферические электронные облака атомов водорода захватываются р-орбиталями вис атома кислорода. Получившие дополнительный отрицательный заряд орбитали вис отталкиваются на угол 104°31'
Внешний слой h имеет шесть электронов (их условное обозначение 2 s2p4, где 2 - номер слоя, s и р - орбитали, индексы 2 и 4 - соответственно количество электронов на орбиталях). В этом слое, как видно из условного обозначения, два s-электрона имеют одну и ту же сферическую орбиталь. Четыре р-электрона вынуждены расположиться на трех взаимно перпендикулярных орбиталях, имеющих в плане формы восьмерок. Восьмерки пересекаются в центре атома, как показано на рис. 10. Обратите внимание: 4 р-электрона на трех орбиталях. Здесь ключ к пониманию всех событий.
Орбиталь, вытянутая вдоль оси г, служит пристанищем для двух электронов. Она укомплектована, и ворота ее на прочном запоре. На орбиталях же х и у по одному электрону и, значит, по одному изготовленному "капкану".
Итак, действующие лица охарактеризованы. Начинается действие.
Вот атом водорода оказался в опасной близости от атома кислорода, и единственный его электрон тотчас же будет захвачен непарной (недоукомплектованной) р-орбиталью. Поскольку у кислорода две непарные орбитали, он способен пленить два атома водорода. При атом сферическое облако водородного s-электрона належится на яйцеобразную ветвь р-орбитали (см. рис. 10).
Между атомами Н и О возникает связь, которая получила название ковалентной. Итогом этой связи и будет возведение весьма своеобразного архитектурного сооружения, известного как Н2О. Своеобразие же образовавшейся молекулы состоит в следующем.
Во-первых, перекрытие электронных облаков приведет к уплотнению области перекрытия и, значит, к росту отрицательного заряда в этой части пространства.
Расположись атомы водорода по обе стороны от ядра атома кислорода под углом 180°, и возникшие уплотнения зарядов никак не отразились бы на электрическом равновесии образовавшейся системы, т.е. центры положительных и отрицательных зарядов по-прежнему находились бы в одной точке - в центре атома кислорода. Но р-орбитали, захватившие водородные электроны, расположены под углом 90°, и поэтому уплотнения в них вызовут смещение центра тяжести отрицательного заряда относительно центра тяжести положительного заряда. Образовавшаяся молекула коды стала одновременно маленьким микромагнитом или, как принято говорить в молекулярной физике, диполе м, способным ориентироваться в магнитном поле.
Во-вторых, ветви р-орбиталей, получившие дополнительные отрицательные заряды, получат и дополнительную силу взаимного отталкивания. Они подальше отодвинутся друг от друга, и угол между ними вместо 90° станет 104°31. Увеличение угла еще более усугубит несимметричность распределения зарядов. В связи с этим дипольный момент молекулы достигнет такой величины, какой не имеют молекулы никаких других веществ на Земле.
И, наконец, в-третьих, сгущение сферического облака s-электрона водородного атома в месте наложения его на р-орбиталь атома кислорода приведет к разрежению этого облака с диаметрально противоположной стороны. Протон водорода, до того равномерно прикрытый сферическим электронным облаком, после "пленения" атомом кислорода окажется оголенным с внешней стороны. Однако ему представляется возможность "прикрыть свою наготу" за счет электронного облака соседней молекулы Н2О. И он сделает это, вцепившись в "одежду" (облако) чужого атома кислорода с силой, которая значительно превзойдет силу, удерживающую его собственный электрон. Эта сила связи с "чужим" атомом кислорода и будет представлять собой так называемую водородную связь.
Золотой ключик
Как вы, вероятно, уже догадались, этим золотым ключиком и являются водородные связи.
Известно, что между двумя любыми достаточно близко расположенными молекулами возникают силы взаимного притяжения: электронная оболочка одной молекулы притягивается положительным зарядом (системой ядер) другой молекулы. Эти силы получили название Ван-дер-Ваальсовых.
Если бы между молекулами воды действовали только Ван-дер-Ваальсовы силы взаимного притяжения, вода замерзала бы при -90°С (183 К), а закипала бы при +80°С (353 К). В действительности вода замерзает при 0°С и закипает при +100°С - обстоятельства, долгое время смущавшие физиков и химиков. Недоумения были рассеяны после открытия водородных связей, более мощных, чем Ван-дер-Ваальсовы.
Водородные связи проявляются не только в воде. Они играют решающую роль в процессе биологического синтеза, т. е. в образовании молекул растительного и живого вещества. Все растущее и живущее на Земле обязано своим существованием специфичности самого распространенного во вселенной элемента - водорода. Однако ни в каком другом веществе водородные связи не проявляются в такой полной мере, как в воде.
Огромный дипольный момент молекул воды и водородные связи объясняют прежде всего аномально высокую диэлектрическую постоянную воды. Если принять диэлектрическую постоянную вакуума за единицу, то диэлектрическая постоянная воды будет равна 80. Это значит, что в воде два электрических заряда будут взаимно притягиваться или отталкиваться с силой, в 80 раз меньше той, с которой они взаимодействовали бы в вакууме.
Высокая диэлектрическая постоянная, в свою очередь, объясняет феноменальную способность воды растворять в себе буквально все вещества, существующие в природе. На Земле не найти абсолютно чистой Н2О. Все воды, включая и дождевую, и родниковую, и многократно дистиллированную, - растворы. Конечно, концентрация растворенных веществ может колебаться в очень широких пределах. Самый распространенный "раствор" на поверхности Земли - морская вода. В каждой ее капле по крайней мере 70 химических элементов таблицы Менделеева, в том числе и самых редких.
Особенно легко растворяются в воде вещества, атомы которых соединены ионной связью. Это сравнительно слабые химические связи. Растворенная в воде, например, поваренная соль легко диссоциирует на ионы натрия (Na+) и хлора (Сl-). Соединиться вновь в воде этим ионам не суждено. Разделенные молекулами воды, они теперь притягиваются друг к другу в 80 раз слабее! К тому же вставшие на их пути молекулы Н2О обладают мощным дипольным моментом и без труда присоединяют к своим отрицательным концам положительные ионы натрия, а отрицательные ионы хлора соответственно исчезают в цепких "лапах" водородных протонов.
Пример растворения солей с ионной связью мы выделили потому, что такие связи составляют основу образования кристаллических структур, а из кристаллических структур в основном и сложена кора Земли, ее материки, горные хребты, дно океанов. Как уж тут не проявиться всеразрушающему свойству воды?
Не следует думать, будто водородные связи намертво удерживают одну молекулу воды относительно, другой. Если бы это случилось, вода при всех условиях оставалась бы сверхпрочным твердым телом. В интервале между 0 и +100 °С водородные связи ослабляют и рвутся под воздействием теплового движения самих молекул воды. Чем больше мы подводим тепла к воде, тем интенсивнее тепловое движение молекул и тем труднее водородным связям удерживать их на близком расстоянии друг подле друга. Наконец, тепловое движение окончательно берет верх над силами водородных связей, молекулы рассыпаются, разлетаются, вода перестает быть жидкостью, она обращается в пар.
