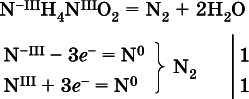Химия. Полный справочник для подготовки к ЕГЭ, стр. 52
сумма коэффициентов равна
1) 3
2) 4
3) 5
4) 6
34—36. В водном растворе соли
34. Са(ClO 4) 2
35. AgF
36. Fe 2(SO 4) 3
образуется среда
1) кислотная
2) нейтральная
3) щелочная
4) любая
37. Концентрация гидроксид-иона увеличивается после растворения в воде соли
1) CsNO 3
2) SrCl 2
3) NaCN
4) KHSO 4
38. Нейтральная среда будет в конечном растворе после смешивания растворов исходных солей в наборах
1) ВаCl 2, Fe(NO 3) 3
2) Na 2CO 3, SrS
3) BaS, ZnSO 4
4) MgCl 2, RbNO 3
39. Установите соответствие между солью и ее способностью к гидролизу.

40. Установите соответствие между солью и средой раствора.

41. Установите соответствие между солью и концентрацией катиона водорода после растворения соли в воде.

14. Окислительно-восстановительные реакции. Электролиз
14.1. Окислители и восстановители
Окислительно-восстановительные реакции протекают с одновременным повышением и понижением степеней окисления элементов и сопровождаются передачей электронов:
Повышениестепени окисления элемента в ходе реакции, отвечающее потереэлектронов атомами этого элемента, называют окислением: S -II– 6е -= S IV. В данном примере S -IIокисляется до S IV.
Понижениестепени окисления элемента в ходе реакции, отвечающее присоединению электронов атомами этого элемента, называется восстановлением: O 0+ 2е -= О -II. В данном примере О 0восстанавливается до O -II.
Вещество, частицы которого содержат окисляющиеся атомы, выполняет в реакции функцию восстановителя.В данном примере восстановитель – сероводород H 2S.
Вещество, частицы которого содержат восстанавливающиеся атомы, выполняет в реакции функцию окислителя.В данном примере окислитель – молекулярный кислород O 2.
Вещества, являющиеся окислителями или восстановителями во многих реакциях, называются типичными (сильными).
Многие вещества могут проявлять как окислительные, так и восстановительные свойства. К таким веществам принадлежат соединения, содержащие элементы в промежуточной (для них) степени окисления:
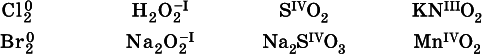
Окислительно-восстановительные свойства веществ связаны с положением элементов в Периодической системе Д. И. Менделеева. Простые вещества – неметаллы обладают бoльшими окислительнымисвойствами, а металлы – бoльшими восстановительнымисвойствами (O 2, Cl 2– окислители; Na, Ва, Al и Zn – восстановители).
В каждой группе Периодической системы элемент с большимпорядковым номером будет обладать и бoльшими восстановительнымисвойствами в своей группе, а элемент с меньшимпорядковым номером – бoльшими окислительнымисвойствами. Так, кальций Са – более сильный восстановитель, чем магний Mg, молекулярный хлор Cl 2– более сильный окислитель, чем иод I 2.
Соединения, содержащие атомы элементов в низкой степени окисления, будут восстановителями за счет этих атомов, например: NH 3– восстановитель за счет азота (-III), H 2S – за счет серы (-II), KI – за счет иода (-I) и т. д.
Соединения, включающие атомы элементов в высокойстепени окисления, будут окислителями, например: HNO 3– окислитель за счет азота (+V), КMnO 4– за счет марганца (+VII), К 2Cr 2O 7– за счет хрома (+VI) и т. д.
14.2. Подбор коэффициентов методом электронного баланса
Метод состоит из нескольких этапов.
1. Записывают схемуреакции; находят элементы, повышающие и понижающие свои степени окисления, и выписывают их отдельно:
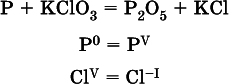
2. Составляют уравнения полуреакцийокисления и восстановления:
3. Подбирают дополнительные множители(справа за чертой) для уравнений полуреакций так, чтобы число электронов, отданных восстановителем, стало равным числу электронов, принятых окислителем:
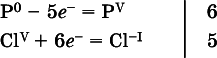
4. Проставляют найденные множителив качестве коэффициентовв схему реакции:
5. Проводят проверку по элементу, который не менял свою степень окисления (чаще всего – кислород):
Примеры:
а)
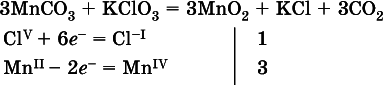
( коэффициентперед СO 2подбирается поэлементно и в последнюю очередь, проверка – по кислороду);
б)
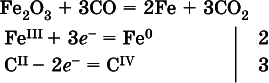
в)
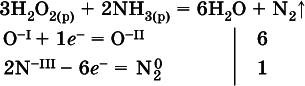
(простые вещества– здесь N 2– пишут в уравнениях полуреакций в молекулярном виде);
г)
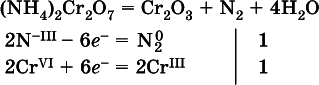
(реакция внутримолекулярногоокисления-восстановления, расчет ведут на число атомов в формульной единице реагента – 2N -IIIи 2Cr VI);
д)
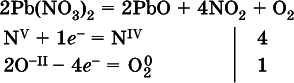
e)
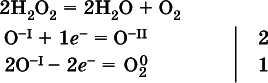
(реакция дисмутации,коэффициенты ставят сначала в правую часть уравнения);
ж)
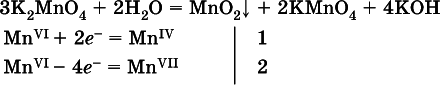
( коэффициентперед К 2MnO 4находят суммированием числа атомов Mn VIв правой части обоих уравнений полуреакций);
з)
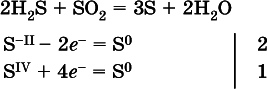
(реакция конмутации,коэффициенты ставят сначала в левую часть уравнения);
и)